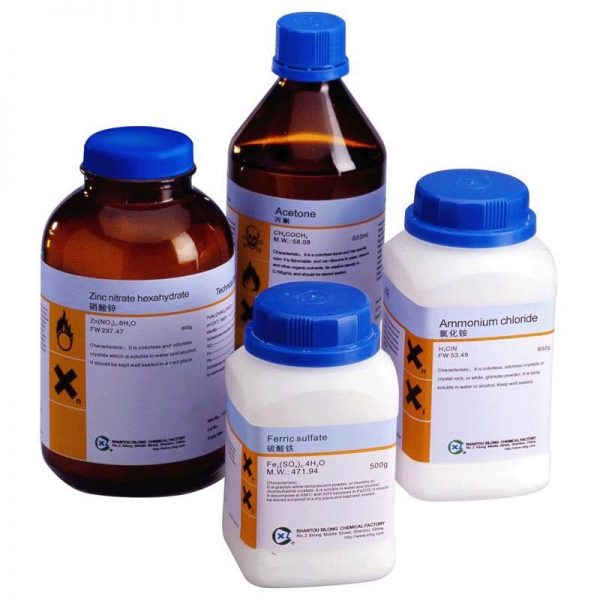
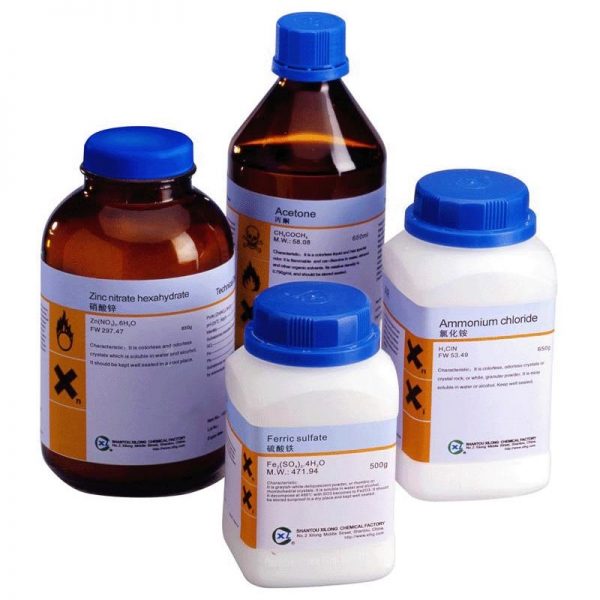
Υδροξείδιο του Μαγνησίου 1kg – Mg(OH)2
Υδροξείδιο του Μαγνησίου 1kg
Το υδροξείδιο του μαγνησίου είναι ανόργανη χημική ένωση με μοριακό τύπο Mg(OH)2 και μοριακό βάρος 58,3197. Είναι γνωστό και ως γάλα μαγνησίας εξαιτίας της μορφής του ως λευκού εναιωρήματος. Παρά το ότι η διαλυτότητά του στο νερό είναι μικρή, είναι αρκετή ώστε να δώσει ιόντα στο διάλυμα, σχηματίζοντας το εναιώρημα. Μία σχετικώς υψηλή συγκέντρωση ιόντων μαγνησίου ή υδροξειδίου θα χρειαζόταν για να μετατρέψει το εναιώρημα σε ίζημα, αντιστρέφοντας την ισορροπία.
Στη μορφή του εναιωρήματος, το υδροξείδιο του μαγνησίου αποτελεί συστατικό αντιόξινων και καθαρτικών φαρμάκων. Επηρεάζει την απορρόφηση του φολικού οξέος και του σιδήρου από τον οργανισμό. Η στερεά μορφή του υδροξειδίου του μαγνησίου απαντάται στη φύση ως το ορυκτό μπρουσίτης.
Φυσικοχημικές Ιδιότητες
Μοριακό βάρος: 58.3197 g/mol
Σημείο Τήξης: 350 °C (662 °F; 623 K)
Πυκνότητα: 2.3446 g/cm3
Διαλυτότητα: 0.00064 g/100 mL (25 °C), 0.004 g/100 mL (100 °C)
Εμφάνιση: Λευκό στερεό
Χημική Δομή
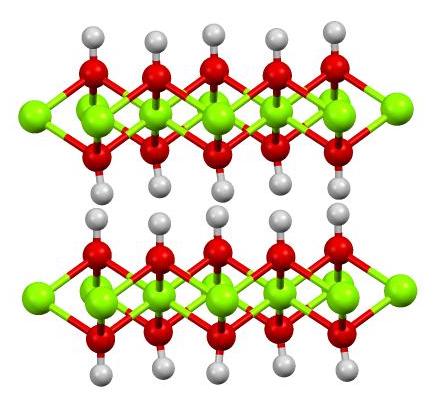
Ασφάλεια και Αποθήκευση
![]()
Προκαλεί ερεθισμό
Φυλάσσεται σε θερμοκρασία δωματίου
Αναλυτική Περιγραφή
Το υδροξείδιο του μαγνησίου σε διάλυμα αποτελείται από κατιόντα μαγνησίου και ανιόντα υδροξυλίου, και θα καθιζάνει όποτε τα δύο συνδυασθούν με μία αντίδραση μετάθεσης. Εξαιτίας της διαθεσιμότητας αλκαλικών αλάτων, αυτό συμβαίνει συνήθως ανάμεσα σε άλατα του μαγνησίου και του νατρίου, του καλίου, ή του αμμωνίου, αλλά μπορεί να συμβεί και σε οποιοδήποτε άλλο βασικό περιβάλλον με παρουσία υδροξυλίου. Η ιοντική αντίδραση είναι η εξής:
- Mg2+ (aq) + 2 OH− (aq) → Mg(OH)2 (s)
Στη φύση το Mg(OH)2 απαντάται με τη μορφή του ορυκτού μπρουσίτη, που χρησιμοποιείται εμπορικά ως επιβραδυντικό πυρκαγιών. Ωστόσο, η μεγαλύτερη ποσότητα υδροξειδίου του μαγνησίου που χρησιμοποιείται στη βιομηχανία παράγεται χημικώς από το θαλασσινό νερό ή την άλμη, και συγκεκριμένα με αντίδραση του χλωριούχου μαγνησίου του θαλάσσιου νερού με ασβεστόλιθο ή δολομίτη, οπότε καθιζάνει υδροξείδιο του μαγνησίου.
Ο μπρουσίτης, η ορυκτή μορφή με την οποία βρίσκεται συνήθως στη φύση το Mg(OH)2, απαντάται στον πηλό και μαζί με χλωρίτη. Στη δεύτερη περίπτωση καταλαμβάνει τις ενδιάμεσες θέσεις που κανονικά καταλαμβάνουνται από μονοσθενή και δισθενή κατιόντα όπως τα Na+, K+, Mg2+ και Ca2+. Ως συνέπεια, οι στρώσεις χλωρίτη «δένονται» από τον μπρουσίτη και δεν μπορούν να διασταλούν ή να συσταλούν πλέον.
Ο μπρουσίτης στον οποίο κάποια κατιόντα Mg2+ έχουν αντικατασταθεί με κατιόντα Al3+ φορτίζεται θετικά και αποτελεί την κύρια συνιστώσα των λεγόμενων διαστρωματωμένων διπλών υδροξειδίων (layered double hydroxide, LDH). Τα ορυκτά LDH, όπως ο υδροταλκίτης, είναι ισχυρά απορροφητικά ανιόντων, αλλά σχετικώς σπάνια στη φύση.
Ο μπρουσίτης μπορεί επίσης να κρυσταλλωθεί επάνω σε τσιμέντο και σκυρόδεμα που έρχονται σε επαφή με θαλάσσιο νερό, καθώς το Mg2+ είναι το δεύτερο αφθονότερο κατιόν στο νερό της θάλασσας μετά το Na+. Ο σχηματισμός μπρουσίτη προκαλεί τοπικές διαστολές στον όγκο, που ευθύνονται για την ανάπτυξη μηχανικών τάσεων στο σκυρόδεμα. Αυτές οι τάσεις δημιουργούν ρωγμές και σχισμές στο σκυρόδεμα, επιταχύνοντας έτσι την υποβάθμισή του στο θαλάσσιο περιβάλλον.
Στις 4 Μαΐου 1818 ένας Αμερικανός ονόματι Τζων Κάλεν (John Callen) κατοχύρωσε δίπλωμα ευρεσιτεχνίας (No. X2952) για το υδροξείδιο του μαγνησίου.
Το 1829 ο Ιρλανδός ιατρός Τζέιμς Μάρεϊ (1788-1871) χρησιμοποίησε υγρό σκεύασμα της ενώσεως για να θεραπεύσει τον αντιβασιλέα της Ιρλανδίας Μαρκήσιο του Anglesey από στομαχικό άλγος, με τόση επιτυχία, ώστε διορίσθηκε προσωπικός ιατρός αυτού και των δύο επόμενων αντιβασιλέων της Ιρλανδίας, και του δόθηκε ο τίτλος του ιππότη (σερ). Το δικής του εμπνεύσεως υγρό σκεύασμα μαγνησίας κατοχυρώθηκε δύο χρόνια μετά τον θάνατό του, το 1873.
Ο όρος «γάλα μαγνησίας» χρησιμοποιήθηκε για πρώτη φορά για ένα λευκό, μετρίως αλκαλικό υδατικό αιώρημα υδροξειδίου του μαγνησίου με συγκέντρωση περίπου 8% κατά βάρος από τον Άγγλο φαρμακοποιό Τσαρλς Χένρυ Φίλιπς το 1872 και άρχισε να πωλείται με την εμπορική ονομασία Phillips’ Milk of Magnesia για ιατρική χρήση.


 Φυσική
Φυσική Χημεία
Χημεία Βιολογία
Βιολογία Μαθηματικά
Μαθηματικά Περιβάλλον – Οικολογία
Περιβάλλον – Οικολογία Επιστήμες της Γης
Επιστήμες της Γης Τεχνολογία
Τεχνολογία Προσχολικά – Σχολικά
Προσχολικά – Σχολικά Ειδική Αγωγή
Ειδική Αγωγή Σχολικός Εξοπλισμός
Σχολικός Εξοπλισμός Τέχνες & Αθλητισμός
Τέχνες & Αθλητισμός Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική
Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική Ψηφιακή Τάξη
Ψηφιακή Τάξη Απαγωγοί
Απαγωγοί Ντουλάπες Φύλαξης
Ντουλάπες Φύλαξης Ψυγεία Καταψύκτες
Ψυγεία Καταψύκτες Εργαστηριακές Συσκευές
Εργαστηριακές Συσκευές Πάγιος Εργαστηριακός Εξοπλισμός
Πάγιος Εργαστηριακός Εξοπλισμός Χημικά Αντιδραστήρια
Χημικά Αντιδραστήρια Ιατρικός – Νοσοκομειακός εξοπλισμός
Ιατρικός – Νοσοκομειακός εξοπλισμός Μικροσκόπια – Στερεοσκόπια
Μικροσκόπια – Στερεοσκόπια USB Αισθητήρες & MBL Αισθητήρες
USB Αισθητήρες & MBL Αισθητήρες STEM EDUCATION
STEM EDUCATION Science School
Science School Εργαστήρια Δεξιοτήτων
Εργαστήρια Δεξιοτήτων Φυσικών Επιστημών Προσχολικής
Φυσικών Επιστημών Προσχολικής Φυσικών Επιστημών Ε & ΣΤ Δημοτικού
Φυσικών Επιστημών Ε & ΣΤ Δημοτικού Πακέτα Ασκήσεων Δευτεροβάθμιας
Πακέτα Ασκήσεων Δευτεροβάθμιας Η Φυσική με Πειράματα – Γυμνασίου
Η Φυσική με Πειράματα – Γυμνασίου Εκπαιδευτικά Σετ
Εκπαιδευτικά Σετ Εκπαιδευτικά Πακέτα Μικροκλίμακας
Εκπαιδευτικά Πακέτα Μικροκλίμακας BeeBot
BeeBot Botzees
Botzees EDISON
EDISON Gigo
Gigo Botley
Botley Spike
Spike Arduino
Arduino MicroBit
MicroBit Raspberry Pi
Raspberry Pi Elecfreaks
Elecfreaks Keyestudio
Keyestudio Fischertechnik
Fischertechnik Grove Πλατφόρμα Ανάπτυξης
Grove Πλατφόρμα Ανάπτυξης DFRobot
DFRobot WaveShare
WaveShare Αισθητήρες
Αισθητήρες Μοτέρ και Ενεργοποιητές
Μοτέρ και Ενεργοποιητές 3D Printing
3D Printing Laser Engraver
Laser Engraver Προσφορές
Προσφορές Drones
Drones