Υδροχλωρικό Οξύ 1Lt 37%
€22,00 με Φ.Π.Α
Υδροχλωρικό Οξύ 1Lt 37% ~11Μ
Υδροχλωρίδιο, Υδροχλώριο, Xλωράνιο, Chlorane, Muriatic acid, Spirits of salt, Hydronium chloride
HCL
M.W. : 36.46(g/mol)
CAS Number : 7647-01-0
https://pubchem.ncbi.nlm.nih.gov/compound/Hydrochloric-acid
Υδροχλωρικό Οξύ 1Lt 37%
Υδροχλωρικό Οξύ 1Lt 37%
Το Υδροχλωρικό Οξύ είναι υδατικό διάλυμα του αέριου υδροχλωρίου με το οποίο έχει και τον ίδιο χημικό τύπο, HCl. Είναι ανόργανο ισχυρό οξύ, πολύ διαβρωτικό με πολλές και σημαντικές βιομηχανικές χρήσεις. Προσβάλλει το δέρμα και καταστρέφει κάθε φυτικό ή ζωικό ιστό. Η οσμή του είναι ερεθιστική και αποπνικτική.
Υδροχλωρικό Οξύ – Υδρογόνο χλωρίδιο (το αέριο) – Σπίρτο του άλατος, κεζάπι
Hydrochloric Acid 1lt 37%
HCL
M.W. : 36.46(g/mol)
CAS Number : 7647-01-0
Το Υδροχλωρικό Οξύ είναι υδατικό διάλυμα του αέριου υδροχλωρίου με το οποίο έχει και τον ίδιο χημικό τύπο, HCl. Είναι ανόργανο ισχυρό οξύ, πολύ διαβρωτικό με πολλές και σημαντικές βιομηχανικές χρήσεις. Προσβάλλει το δέρμα και καταστρέφει κάθε φυτικό ή ζωικό ιστό. Η οσμή του είναι ερεθιστική και αποπνικτική.
Φυσικοχημικές Ιδιότητες
Μοριακός Τύπος: HCl
Μοριακό βάρος: 36.46 g·mol−1
Εμφάνιση/οσμή: άχρωμο υγρό, με ατμούς σε μεγάλη συγκέντρωση
Σημείο ζέσης: 71 °C (σε αυτή τη συγκέντρωση, 35%)
Σημείο τήξης: −36 °C (σε αυτή τη συγκέντρωση, 35%)
Πυκνότητα: 1.169 g cm−3
Χημική Δομή
![]()
Ασφάλεια και αποθήκευση

Διαβρωτικό Τοξικό
Αναλυτική περιγραφή
Το μόριο του υδροχλωρίου είναι διατομικό και αποτελείται από ένα άτομο υδρογόνου (H) και ένα άτομο χλωρίου (Cl), που συνδέονται με απλό ομοιοπολικό δεσμό. Δεδομένου ότι το άτομο του χλωρίου είναι πολύ πιο ηλεκτροαρνητικό από το άτομο του υδρογόνου, ο δεσμός μεταξύ των δύο ατόμων είναι έντονα πολωμένος. Κατά συνέπεια, το μόριο έχει μεγάλη διπολική ροπή, με το στοιχειώδες αρνητικό φορτίο (δ–) να αποδίδεται στο άτομο χλωρίου και το θετικό (δ+) στο άτομο του υδρογόνου. Λόγω της μεγάλης του πολικότητας, το HCl είναι πολύ διαλυτό στο νερό (αλλά και σε άλλους πολικούς διαλύτες).
Το στερεοποιημένο HCl αλλάζει φάση δομής σε θερμοκρασία κάτω από 98,4 K. Η περίθλαση ακτίνων Χ σε σκόνη στερεού HCl δείχνει ότι αλλάζει από ορθορομβική δομή σε κυβική δομή κατά τη μετάβαση αυτής της της θερμοκρασίας.





 Φυσική
Φυσική Χημεία
Χημεία Βιολογία
Βιολογία Μαθηματικά
Μαθηματικά Περιβάλλον – Οικολογία
Περιβάλλον – Οικολογία Επιστήμες της Γης
Επιστήμες της Γης Τεχνολογία
Τεχνολογία Προσχολικά – Σχολικά
Προσχολικά – Σχολικά Ειδική Αγωγή
Ειδική Αγωγή Σχολικός Εξοπλισμός
Σχολικός Εξοπλισμός Τέχνες & Αθλητισμός
Τέχνες & Αθλητισμός Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική
Χειροτεχνία – Χαρτικά – Γραφική ύλη – Ζωγραφική Labdisc
Labdisc Ψηφιακή Τάξη
Ψηφιακή Τάξη Απαγωγοί
Απαγωγοί Ντουλάπες Φύλαξης
Ντουλάπες Φύλαξης Ψυγεία Καταψύκτες
Ψυγεία Καταψύκτες Εργαστηριακές Συσκευές
Εργαστηριακές Συσκευές Πάγιος Εργαστηριακός Εξοπλισμός
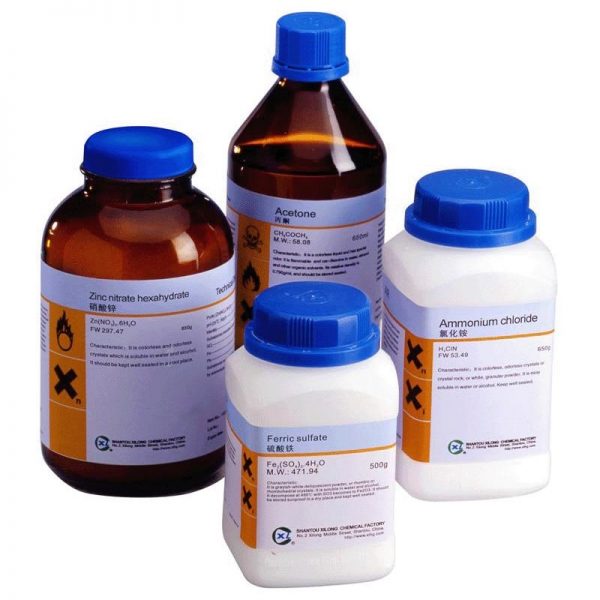
Πάγιος Εργαστηριακός Εξοπλισμός Χημικά Αντιδραστήρια
Χημικά Αντιδραστήρια Ιατρικός – Νοσοκομειακός εξοπλισμός
Ιατρικός – Νοσοκομειακός εξοπλισμός Μικροσκόπια – Στερεοσκόπια
Μικροσκόπια – Στερεοσκόπια USB & MBL & Wireless Αισθητήρες
USB & MBL & Wireless Αισθητήρες STEM EDUCATION
STEM EDUCATION Science School
Science School Εργαστήρια Δεξιοτήτων
Εργαστήρια Δεξιοτήτων Φυσικών Επιστημών Προσχολικής
Φυσικών Επιστημών Προσχολικής Φυσικών Επιστημών Ε & ΣΤ Δημοτικού
Φυσικών Επιστημών Ε & ΣΤ Δημοτικού Πακέτα Ασκήσεων Δευτεροβάθμιας
Πακέτα Ασκήσεων Δευτεροβάθμιας Η Φυσική με Πειράματα – Γυμνασίου
Η Φυσική με Πειράματα – Γυμνασίου Εκπαιδευτικά Σετ
Εκπαιδευτικά Σετ Εκπαιδευτικά Πακέτα Μικροκλίμακας
Εκπαιδευτικά Πακέτα Μικροκλίμακας BeeBot
BeeBot Botzees
Botzees EDISON
EDISON Gigo
Gigo Botley – Kitt
Botley – Kitt Spike
Spike Εξοπλισμός Υπουργείου
Εξοπλισμός Υπουργείου Εξοπλισμός Σχολείων 1821
Εξοπλισμός Σχολείων 1821 Ρομπότ Τηλεπαρουσίασης
Ρομπότ Τηλεπαρουσίασης DOBOT
DOBOT VR Τεχνολογικά
VR Τεχνολογικά Arduino
Arduino MicroBit
MicroBit Raspberry Pi
Raspberry Pi Elecfreaks
Elecfreaks Keyestudio
Keyestudio Fischertechnik
Fischertechnik Makerzoid
Makerzoid Grove Πλατφόρμα Ανάπτυξης
Grove Πλατφόρμα Ανάπτυξης DFRobot
DFRobot WaveShare
WaveShare Αισθητήρες
Αισθητήρες Μοτέρ και Ενεργοποιητές
Μοτέρ και Ενεργοποιητές 3D Printing
3D Printing Laser Engraver
Laser Engraver Προσφορές
Προσφορές Drones
Drones